istoric –
Tratamentul de referință activează o altă proteină din sânge care previne secerizarea.

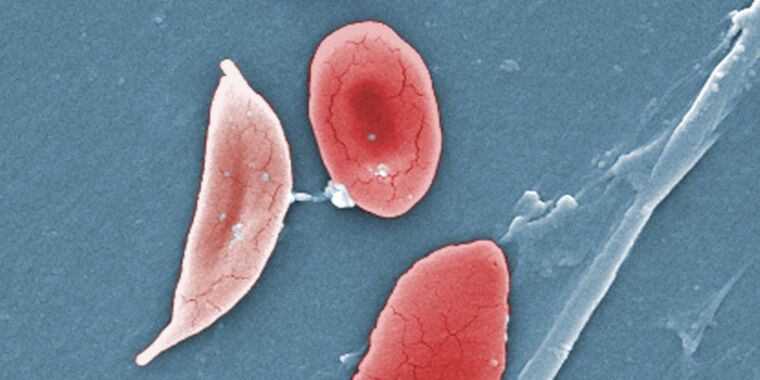
Mărește / Această micrografie electronică cu scanare colorată digital (SEM) a dezvăluit o parte din morfologia ultrastructurală comparativă dintre celulele roșii din sânge (RBC) normale și un RBC de celule secera (stânga) găsit într-un eșantion de sânge al unei paciente de 18 ani cu celule secera. anemie.
Administrația pentru Alimente și Medicamente vineri a aprobat două terapii genetice pentru a trata boala cu celule seceraunul dintre acestea fiind primul tratament bazat pe CRISPR/Cas9 care a câștigat aprobarea de reglementare în SUA.
Anunțul este un punct de reper în tratamentul siclemiei, o afecțiune devastatoare în care celulele roșii din sânge se deformează în formă de seceră și înfundă vasele de sânge. Siclemia afectează aproximativ 100.000 de oameni din SUA, cel mai frecvent afro-americani. Ea duce la anemie, evenimente vaso-ocluzive și crize (episoade dureroase în care mici blocaje înfometează țesutul de oxigen), accidente vasculare cerebrale, leziuni progresive și ireversibile ale organelor, scăderea calității vieții și moarte timpurie.
Până astăzi, tratamentele au fost limitate. Un transplant de măduvă osoasă de la un frate cu potrivire genetică poate vindeca afecțiunea mai mult de 90 la sută din timp, dar doar aproximativ 20 la sută dintre persoanele cu boală au un astfel de donator de frați potriviți genetic. Există, de asemenea, mai multe medicamente disponibile și îngrijire de susținere, dar acestea reduc în principal severitatea bolii. Noile tratamente de terapie genică, pe de altă parte, s-au dovedit a fi foarte eficiente în prevenirea evenimentelor și crizelor vaso-ocluzive.
„Drepanocitoarea este o afecțiune a sângelui rară, debilitantă și care pune viața în pericol, cu nevoi semnificative nesatisfăcute și suntem încântați să avansăm în domeniu, în special pentru persoanele ale căror vieți au fost grav perturbate de boală, prin aprobarea a două terapii genetice bazate pe celule. astăzi”, a declarat Nicole Verdun, directorul Biroului de Produse Terapeutice din cadrul Centrului de Evaluare și Cercetare a Produselor Biologice al FDA, în anunțul FDA.
Pentru a înțelege modul în care funcționează terapiile genetice, este util să înțelegem ce cauzează boala secerată. Problema centrală este cu hemoglobina adultului, proteina care conține fier din celulele roșii din sânge care transportă oxigenul de la plămâni la restul corpului. La pacienții cu siclemie, există o singură mutație mică a genei care codifică hemoglobina. Mutația este un comutator al unei singure nucleotide, sau bază, (deseori reprezentată de literele A, C, T și G). Trecerea unui A la T în codul genetic pentru hemoglobină are ca rezultat o proteină a hemoglobinei cu o valină în loc de un acid glutamic în poziția a șasea aminoacid. Aceasta transformă hemoglobina adultă normală (HbA) în hemoglobină falcioasă (HbS). În celulele roșii din sânge, atunci când HbS pierde oxigenul pe care îl transporta, se polimerizează cu ea însăși, formând structuri asemănătoare șuvițelor care deformează celula.
Editări eficiente
Terapia CRISPR/Cas9 aprobată astăzi, numită Casgevy, previne această deformare activând în esență producția unui alt tip de hemoglobină codificată în modelele noastre genetice – hemoglobina fetală (HbF). HbF este optimizat pentru sarcină, transferând oxigen din sângele matern în țesutul fetal, iar gena care îl codifică este oprită la scurt timp după naștere, pe măsură ce organismul trece la HbA. La aproximativ șase luni după naștere, HbF reprezintă de obicei doar 1% până la 2% din hemoglobina din organism.
Dar, HbF poate trata eficient boala cu celule falciforme – hemoglobina transportă oxigenul foarte bine la adulți și nu se polimerizează. Mai mult, atunci când este amestecat cu HbS, împiedică polimerizarea proteinei mutante cu ea însăși, împiedicând-o să formeze structuri care deformează celulele roșii din sânge.
Casgevy pornește HbF cu sistemul CRISPR/Cas9, un sistem de editare genetică inițial ștearsă de bacterii care tăie ADN-ul folosind o enzimă (o nuclează) numită Cas9. Cas9 poate fi direcționat către porțiuni specifice de ADN folosind o secvență scurtă de ghidare a ARN. În Casgevy, sistemul CRISPR/Cas9 este direcționat pentru a tăia o genă care codifică o proteină numită BCL11A, care controlează alte gene, denumite un factor de transcripție. Factorul de transcripție BCL11A este proteina responsabilă pentru oprirea genei pentru HbF la scurt timp după naștere, pe măsură ce organismul trece la versiunea adultă. Cu snip-ul CRISPR/Cas9, BCL11A este oprit, iar producția de HbF poate relua.
Pentru pacienții care sunt tratați, acest proces implică mai întâi recoltarea de celule stem din măduva osoasă, care apoi primesc CRISPR într-un laborator specializat. Între timp, pacienții primesc chimioterapie pentru a ucide celulele măduvei osoase pentru a face loc celulelor modificate genetic, care sunt apoi reintroduse. Din cei 31 de pacienți tratați cu Cagevy și urmăriți timp de cel puțin 24 de luni, 29 (93,5 la sută) au trecut cel puțin 12. luni consecutive fără criză vaso-ocluzivă.
Cealaltă terapie genică aprobată astăzi de FDA este Lyfgenia, care a folosit un vector lentiviral pentru a introduce gene în genomul uman. În acest caz, sistemul furnizează codul genetic pentru un tip modificat de hemoglobină care este proiectat să fie anti-falciform, numit HbA.T87Q. Dintre 32 de pacienți tratați cu Lyfgenia, 28 (88%) nu au avut evenimente vaso-ocluzive timp de șase până la 18 luni după tratament.
Ambele terapii genice sunt aprobate pentru pacienții cu vârsta de peste 12 ani.